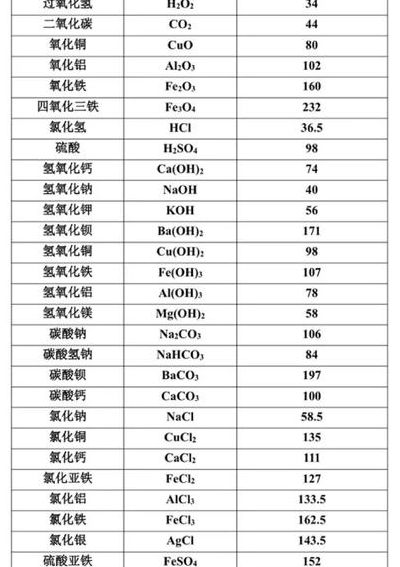
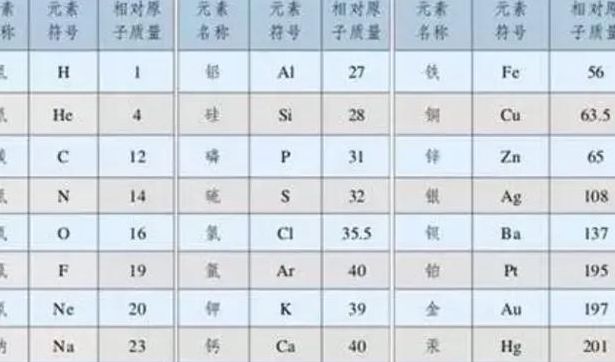
碘的相对分子质量和相对原子质量都是127吗?为什么?I不是以分子形式存在...
碘的相对原子质量是129,而不是127。相对原子质量是一个原子的质量与碳-12同位素质量的1/12的比值,碘的原子质量接近129,因此其相对原子质量被定为129。碘的相对分子质量是258,这是因为碘通常以I分子的形式存在。相对分子质量是构成分子的各原子的相对原子质量的总和。
不是,碘单质通常以I分子的形式存在。碘相对原子质量129,碘相对分子质量258。碘元素是原子量为129的非金属化学元素,原子序数为53,一般分子式为I,式量258。化学性质较活泼,非金属性强,是一种人类必须的微量元素。碘与人类的健康息息相关。
碘的相对原子质量是127,碘单质通常以I2分子的形式存在,所以它的相对分子质量是25元素周期表53号元素碘,在化学元素周期表中位于5周期系ⅦA族是卤族元素之一。1811年法国药剂师库特瓦首次发现单质碘。单质碘呈紫黑色晶体,易升华,升华后易凝华。有毒性和腐蚀性。碘单质遇淀粉会变蓝紫色。
碘相对原子质量等于
1、碘的相对原子质量是1290447。相对原子质量是一个元素所有同位素质量的加权平均值与碳-12同位素质量之比。碘是一种非金属元素,在化学和生物学中具有重要的应用。它具有多个同位素,其中最稳定的是碘-127。了解碘的相对原子质量有助于理解该元素在化学反应和核反应中的性质和行为。
2、碘的相对原子质量是129,而不是127。相对原子质量是一个原子的质量与碳-12同位素质量的1/12的比值,碘的原子质量接近129,因此其相对原子质量被定为129。碘的相对分子质量是258,这是因为碘通常以I分子的形式存在。相对分子质量是构成分子的各原子的相对原子质量的总和。
3、碘的相对原子质量是127,碘是一种非金属化学元素,元素符号是I,原子序是53,碘是最重的非人造稳定的卤素元素,在标准状况下以有光泽的紫黑色固态非金属存在,在摄氏114度时融化成深紫黑色液体,在摄氏184度时挥发成深紫罗兰色气体。
4、碘的相对原子质量是127,碘单质通常以I2分子的形式存在,所以它的相对分子质量是25元素周期表53号元素碘,在化学元素周期表中位于5周期系ⅦA族是卤族元素之一。1811年法国药剂师库特瓦首次发现单质碘。单质碘呈紫黑色晶体,易升华,升华后易凝华。有毒性和腐蚀性。碘单质遇淀粉会变蓝紫色。
5、碘的相对原子质量是127,碘单质通常以I2分子的形式存在,所以它的相对分子质量是254。碘是一种紫黑色有光泽的片状晶体,原子序数53,自然界存在的同位素是74个中子的碘-127。碘具有较高的蒸汽压,在微热下即升华,纯碘蒸气呈深蓝色,若含有空气则呈紫红色,并有刺激性气味。
6、碘原子的相对原子质量是129,是根据碘在自然界中各种同位素的存在比例加权平均得出的数值。在化学中,我们常用相对原子质量来表示一个元素的质量。碘(符号:I)是位于元素周期表第17组的一种卤素元素。它的原子编号为53,具有多种同位素,其中最稳定的是碘-127。
碘相对原子质量
碘的相对原子质量是129,而不是127。相对原子质量是一个原子的质量与碳-12同位素质量的1/12的比值,碘的原子质量接近129,因此其相对原子质量被定为129。碘的相对分子质量是258,这是因为碘通常以I分子的形式存在。相对分子质量是构成分子的各原子的相对原子质量的总和。
碘的相对原子质量是129034。下面进行详细的解释:相对原子质量是指一个原子的质量与碳原子质量的十二分之一的比值。这是一种相对数值,用来表示不同原子的质量相对于碳原子质量的比值大小。碘的相对原子质量是其在自然界中广泛存在的同位素平均计算出来的结果。
碘的相对原子质量是129。以下是 相对原子质量是指以一个碳原子的质量的十二分之一作为标准,其他元素的原子质量相对于这一标准的比值,也称为相对原子质量。对于碘元素来说,它的相对原子质量是经过科学测定得出的结果。碘是一种化学元素,在元素周期表中处于第五周期的位置。
碘的相对原子质量是1290447。相对原子质量 定义:相对原子质量是一个元素的平均原子质量与碳-12同位素的质量之比。它通常以标准原子质量单位(u)表示。计算方法:相对原子质量可以通过计算一个元素所有同位素的原子质量的加权平均值得到,其中加权因子是各同位素的丰度。
碘的相对原子质量是127,碘是一种非金属化学元素,元素符号是I,原子序是53,碘是最重的非人造稳定的卤素元素,在标准状况下以有光泽的紫黑色固态非金属存在,在摄氏114度时融化成深紫黑色液体,在摄氏184度时挥发成深紫罗兰色气体。
碘原子的相对原子质量是129,是根据碘在自然界中各种同位素的存在比例加权平均得出的数值。在化学中,我们常用相对原子质量来表示一个元素的质量。碘(符号:I)是位于元素周期表第17组的一种卤素元素。它的原子编号为53,具有多种同位素,其中最稳定的是碘-127。
碘的相对原子质量是多少?
1、碘的相对原子质量是129,而不是127。相对原子质量是一个原子的质量与碳-12同位素质量的1/12的比值,碘的原子质量接近129,因此其相对原子质量被定为129。碘的相对分子质量是258,这是因为碘通常以I分子的形式存在。相对分子质量是构成分子的各原子的相对原子质量的总和。
2、碘的相对原子质量是129034。下面进行详细的解释:相对原子质量是指一个原子的质量与碳原子质量的十二分之一的比值。这是一种相对数值,用来表示不同原子的质量相对于碳原子质量的比值大小。碘的相对原子质量是其在自然界中广泛存在的同位素平均计算出来的结果。
3、碘的相对原子质量是129。以下是 相对原子质量是指以一个碳原子的质量的十二分之一作为标准,其他元素的原子质量相对于这一标准的比值,也称为相对原子质量。对于碘元素来说,它的相对原子质量是经过科学测定得出的结果。碘是一种化学元素,在元素周期表中处于第五周期的位置。
4、碘原子的相对原子质量是129,是根据碘在自然界中各种同位素的存在比例加权平均得出的数值。在化学中,我们常用相对原子质量来表示一个元素的质量。碘(符号:I)是位于元素周期表第17组的一种卤素元素。它的原子编号为53,具有多种同位素,其中最稳定的是碘-127。
碘的相对原子质量是多少
1、碘的相对原子质量是129,而不是127。相对原子质量是一个原子的质量与碳-12同位素质量的1/12的比值,碘的原子质量接近129,因此其相对原子质量被定为129。碘的相对分子质量是258,这是因为碘通常以I分子的形式存在。相对分子质量是构成分子的各原子的相对原子质量的总和。
2、碘的相对原子质量是129。以下是 相对原子质量是指以一个碳原子的质量的十二分之一作为标准,其他元素的原子质量相对于这一标准的比值,也称为相对原子质量。对于碘元素来说,它的相对原子质量是经过科学测定得出的结果。碘是一种化学元素,在元素周期表中处于第五周期的位置。
3、碘的相对原子质量是129034。下面进行详细的解释:相对原子质量是指一个原子的质量与碳原子质量的十二分之一的比值。这是一种相对数值,用来表示不同原子的质量相对于碳原子质量的比值大小。碘的相对原子质量是其在自然界中广泛存在的同位素平均计算出来的结果。
4、碘的相对原子质量是127,碘是一种非金属化学元素,元素符号是I,原子序是53,碘是最重的非人造稳定的卤素元素,在标准状况下以有光泽的紫黑色固态非金属存在,在摄氏114度时融化成深紫黑色液体,在摄氏184度时挥发成深紫罗兰色气体。
5、碘的相对原子质量是1290447。相对原子质量 定义:相对原子质量是一个元素的平均原子质量与碳-12同位素的质量之比。它通常以标准原子质量单位(u)表示。计算方法:相对原子质量可以通过计算一个元素所有同位素的原子质量的加权平均值得到,其中加权因子是各同位素的丰度。
6、碘原子的相对原子质量是129,是根据碘在自然界中各种同位素的存在比例加权平均得出的数值。在化学中,我们常用相对原子质量来表示一个元素的质量。碘(符号:I)是位于元素周期表第17组的一种卤素元素。它的原子编号为53,具有多种同位素,其中最稳定的是碘-127。
碘的相对原子质量
碘的相对原子质量是129,而不是127。相对原子质量是一个原子的质量与碳-12同位素质量的1/12的比值,碘的原子质量接近129,因此其相对原子质量被定为129。碘的相对分子质量是258,这是因为碘通常以I分子的形式存在。相对分子质量是构成分子的各原子的相对原子质量的总和。
碘的相对原子质量是129034。下面进行详细的解释:相对原子质量是指一个原子的质量与碳原子质量的十二分之一的比值。这是一种相对数值,用来表示不同原子的质量相对于碳原子质量的比值大小。碘的相对原子质量是其在自然界中广泛存在的同位素平均计算出来的结果。
碘的相对原子质量是129。以下是 相对原子质量是指以一个碳原子的质量的十二分之一作为标准,其他元素的原子质量相对于这一标准的比值,也称为相对原子质量。对于碘元素来说,它的相对原子质量是经过科学测定得出的结果。碘是一种化学元素,在元素周期表中处于第五周期的位置。
碘的相对原子质量是1290447。相对原子质量 定义:相对原子质量是一个元素的平均原子质量与碳-12同位素的质量之比。它通常以标准原子质量单位(u)表示。计算方法:相对原子质量可以通过计算一个元素所有同位素的原子质量的加权平均值得到,其中加权因子是各同位素的丰度。
碘原子的相对原子质量是129,是根据碘在自然界中各种同位素的存在比例加权平均得出的数值。在化学中,我们常用相对原子质量来表示一个元素的质量。碘(符号:I)是位于元素周期表第17组的一种卤素元素。它的原子编号为53,具有多种同位素,其中最稳定的是碘-127。
文章声明:以上内容(如有图片或视频亦包括在内)除非注明,否则均为网友提供,转载或复制请以超链接形式并注明出处。