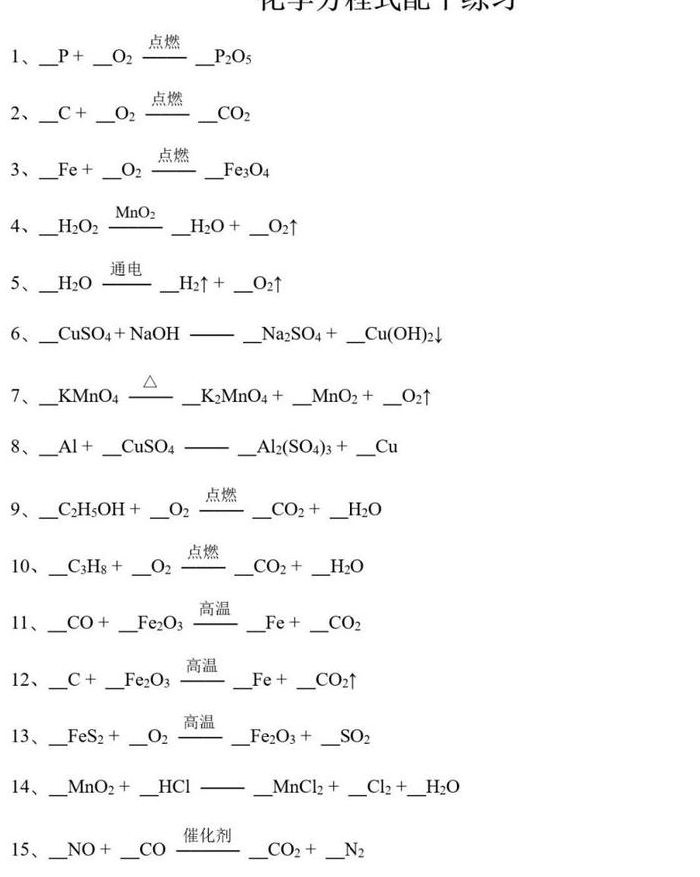化学方程式如何配平
1、如果我们只根据质量守恒配平,得到的反应方程式应该是:Fe+Fe^3+=2Fe^2+,但是我们可以看到,如果这样配平,反应前是3个正电荷,反应后却是4个了,所以是不对的。正确的应该是:Fe+2Fe^3+→3Fe^2+,既满足了质量守恒,也满足了电荷守恒。化学方程式配平的方法 一般都是根据化合价来配平。
2、化学方程式配平的方法如下:分数配平法:有单质参加反应或有单质生成的化学反应方程式的“万能配平法”,即先将化学方程式中“单质外”元素原子配平,最后再添加适当分数配平“单质”元素原子。
3、奇偶配平法:此方法适用于化学方程式两边某一元素多次出现,并且两边该元素原子总数有一奇一偶。电子得失法:从反应式里找出氧化剂和还原剂,并表明被氧化元素或还原元素的原子在反应前后化合价发生变化的情况,以便确定电子得失数。最小公倍数法:这种方法适合于常见的难度不大的化学方程式。
4、化学方程式配平的方法有:零价法用法、平均标价法用法、整体标价法用法、逆向配平法。零价法用法:无法用常规方法确定化合价的物质中各元素均为零价,然后计算出各元素化合价的升降值,并使元素化合价升降值相等,最后用观察法配平其他物质的化学计量数。
化学方程式怎么配平?简单点
例如,甲醇(CH3OH)燃烧化学方程式的配平可采用此法:CH3OH+O2→H2O+CO2。显然,决定生成H2O与CO2的多少的关键是甲醇的组成,因此定其计量数为1,这样可得其燃烧后生成H2O与CO2的分子个数:CH3OH+O2→2H2O+CO2。
质量守恒 也就是说方程式前后的相同原子的数目要相同。
奇偶配平法:此方法适用于化学方程式两边某一元素多次出现,并且两边该元素原子总数有一奇一偶。电子得失法:从反应式里找出氧化剂和还原剂,并表明被氧化元素或还原元素的原子在反应前后化合价发生变化的情况,以便确定电子得失数。最小公倍数法:这种方法适合于常见的难度不大的化学方程式。
化学方程式配平的方法如下:分数配平法:有单质参加反应或有单质生成的化学反应方程式的“万能配平法”,即先将化学方程式中“单质外”元素原子配平,最后再添加适当分数配平“单质”元素原子。
化学方程式怎样配平?
化学方程式配平的方法如下:分数配平法:有单质参加反应或有单质生成的化学反应方程式的“万能配平法”,即先将化学方程式中“单质外”元素原子配平,最后再添加适当分数配平“单质”元素原子。
如果我们只根据质量守恒配平,得到的反应方程式应该是:Fe+Fe^3+=2Fe^2+,但是我们可以看到,如果这样配平,反应前是3个正电荷,反应后却是4个了,所以是不对的。正确的应该是:Fe+2Fe^3+→3Fe^2+,既满足了质量守恒,也满足了电荷守恒。化学方程式配平的方法 一般都是根据化合价来配平。
如果是氧化还原反应,一般用升降法配平。化合价升降配平法,是根据得失电子守恒、电荷守恒、质量守恒定理来进行化学式配平。化合价升高的总数等于化合价下降的总数,即得失电子守恒。 反应式等号两边阴阳离子所带电荷总数相等,即电荷守恒。反应前后各元素的原子个数相等,即质量守恒。
化学方程式配平的方法有:零价法用法、平均标价法用法、整体标价法用法、逆向配平法。零价法用法:无法用常规方法确定化合价的物质中各元素均为零价,然后计算出各元素化合价的升降值,并使元素化合价升降值相等,最后用观察法配平其他物质的化学计量数。
定一法需要找到化学方程式中关键的化学式,定其化学式前计量数为1,然后根据关键化学式去配平其他化学式前的化学计量数。若出现计量数为分数,再将各计量数同乘以同一整数,化分数为整数,这种先定关键化学式计量数为1的配平方法,称为定一法。
配平方程式的方法如下:最小公倍数法:求出方程式两边相同原子前系数的最小公倍数,然后用该最小公倍数除以各自的原子个数,所得的值就是对应物质的系数。观察法:适用于一些简单的方程式,用观察法配平的关键是搞清反应的实质。
文章声明:以上内容(如有图片或视频亦包括在内)除非注明,否则均为网友提供或互联网,转载或复制请以超链接形式并注明出处。