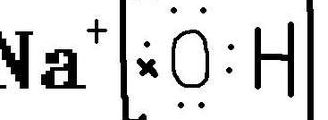氢氧化钠的电子式
氢氧化钠的电子式如图所示:氢氧化钠的性质:氢氧化钠具有强碱性与吸湿性。易溶于水,溶解时放热,水溶液呈碱性。腐蚀性极强,对纤维、皮肤、玻璃、陶瓷等有腐蚀作用。与金属铝和锌、非金属硼和硅等反应放出氢;与氯、溴、碘等卤素发生歧化反应;与酸类起中和作用而生成盐和水。
氢氧化钠的电子式为 Na+[:OH]-。氢氧化钠的电子式的定义 氢氧化钠的电子式为Na+[:OH]-,表示钠离子和氢氧根离子通过得失电子结合在一起,形成离子键。氢氧化钠,化学式为NaOH,俗称烧碱、火碱、苛性钠,是一种具有强腐蚀性的强碱,一般为片状和块状形态,易溶于水。
氢氧化钠的电子式为Na+[:O:H]-。具体来说,Na+代表钠离子,而[:O:H]-则代表氢氧根离子。在这个电子式中,氧原子周围有8个电子,氢原子则有2个电子。氢氧原子间以共价键连接。这样的表示方式只适用于主族元素形成的物质,并不适用于过渡元素形成的物质。
氢氧化钠的电子式可以写为Na+[OH]-。这里,[OH]表示氢氧根离子,由一个氧原子和两个氢原子组成。在氢氧化钠中,钠离子(Na+)和氢氧根离子之间形成离子键,而氢氧根离子内部则存在共价键。氢氧化钠是一种典型的离子化合物,因此它的电子式主要由离子键组成。
溶剂再生装置
溶剂再生装置是一种用于回收有机溶剂的设备,其中乙醇胺常被用作吸收硫化氢的溶剂。乙醇胺浓度对硫化氢吸收效果会产生影响。一般来说,乙醇胺浓度越高,则其对硫化氢的吸收能力也就越强。这是因为在高浓度下,乙醇胺分子之间的相互作用力增大,从而使得其分子更容易与硫化氢发生反应并形成稳定的络合物。
有机废气处理-废气洗涤塔:洗涤塔对于处理酸(碱)雾的废气的净化效率高,净化效率可高达95%,且可以处理印染、医药、喷漆厂、喷漆厂、轻工废气、化工厂等的废气处理,设备在运行时的阻力小,相对于活性炭吸附装置较为节能环保。
催化重整装置:用直馏汽油(即石脑油)或二次加工汽油的混合油作原料,在催化剂(铂或多金属)的作用下,经过脱氢环化、加氢裂化和异构化等反应,使烃类分子重新排列成新的分子结构,以生产C6~C9芳烃产品或高辛烷值汽油为主要目的,并利用重整副产氢气供二次加工的热裂化、延迟焦化的汽油或柴油加氢精制。
氢氧化钠电子式
1、氢氧化钠的电子式为 Na+[:OH]-。氢氧化钠的电子式的定义 氢氧化钠的电子式为Na+[:OH]-,表示钠离子和氢氧根离子通过得失电子结合在一起,形成离子键。氢氧化钠,化学式为NaOH,俗称烧碱、火碱、苛性钠,是一种具有强腐蚀性的强碱,一般为片状和块状形态,易溶于水。
2、氢氧化钠的电子式如图所示:氢氧化钠的性质:氢氧化钠具有强碱性与吸湿性。易溶于水,溶解时放热,水溶液呈碱性。腐蚀性极强,对纤维、皮肤、玻璃、陶瓷等有腐蚀作用。与金属铝和锌、非金属硼和硅等反应放出氢;与氯、溴、碘等卤素发生歧化反应;与酸类起中和作用而生成盐和水。
3、氢氧化钠的电子式如图所示 氢氧化钠 氢氧化钠,化学式为NaOH,俗称烧碱、火碱、苛性钠,为一种具有强腐蚀性的强碱,一般为片状或块状形态,易溶于水(溶于水时放热)并形成碱性溶液,另有潮解性,易吸取空气中的水蒸气(潮解)和二氧化碳(变质),可加入盐酸检验是否变质。
4、naoh的电子式是Na+[:O:H]-。NaOH是氢氧化钠,又称烧碱和苛性钠。为一种具有很强腐蚀性的强碱,一般为片状或颗粒形态,易溶于水,溶于水时放热并形成碱性溶液,另有潮解性,易吸取空气中的水蒸气和二氧化碳。
5、Na+(OH)-。氢氧化钠NaOH是离子化合物,钠离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键。因此,氢氧化钠电子式的书写为:Na+(OH)-。
氢氧化钠的形成的电子式?
1、氢氧化钠的形成过程可以分为苛化法、电解法,其电子式表示如下:苛化法:Na2CO3+Ca(OH)2→2NaOH+CaCO3↓ Na2CO3+Ca(OH)2→2NaOH+CaCO3↓ , NaHCO3+Ca(OH)2→NaOH+CaCO3↓+H2O。电解法:2NaCl+2H2O[电解]→2NaOH+Cl2↑+H2↑。2NaCl+2H2O→2NaOH+H2↑+Cl2↑。
2、氢氧化钠的形成过程电子式:2Na-2(e-)→2Na+ 2H2O+2(e-)→OH-+H2↑ 氢氧化钠,化学式为NaOH,为一种具有强腐蚀性的强碱,一般为片状或块状形态,易溶于水(溶于水时放热)并形成碱性溶液,另有潮解性,易吸取空气中的水蒸气(潮解)和二氧化碳(变质),可加入盐酸检验是否变质。
3、能。氢氧化钠的形成过程电子式:2Na-2(e-)-2Na+2H2O+2(e-)-OH-+H2↑。氢氧化钠,也称苛性钠、烧碱、火碱,是一种无机化合物,化学式NaOH,氢氧化钠具有强碱性,腐蚀性极强,可作酸中和剂、配合掩蔽剂、沉淀剂、沉淀掩蔽剂、显色剂、皂化剂、去皮剂、洗涤剂等。
4、是的,NaOH形成的是离子键,它的电子式是Na+[:O:-H]+。以下是详细的解释:氢氧化钠是一种典型的离子化合物,由钠离子和氢氧根离子组成。钠原子倾向于失去一个电子,形成正电荷的钠离子,而氧原子和氢原子则通过接受电子形成负一价的氢氧根离子,两者之间的相互作用形成离子键。
5、氢氧化钠的电子式为 Na+[:OH]-。氢氧化钠的电子式的定义 氢氧化钠的电子式为Na+[:OH]-,表示钠离子和氢氧根离子通过得失电子结合在一起,形成离子键。氢氧化钠,化学式为NaOH,俗称烧碱、火碱、苛性钠,是一种具有强腐蚀性的强碱,一般为片状和块状形态,易溶于水。
氢氧化钠的电子式怎么写
Na+(OH)-。氢氧化钠NaOH是离子化合物,钠离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键。因此,氢氧化钠电子式的书写为:Na+(OH)-。
氢氧化钠的电子式如图所示:氢氧化钠的性质:氢氧化钠具有强碱性与吸湿性。易溶于水,溶解时放热,水溶液呈碱性。腐蚀性极强,对纤维、皮肤、玻璃、陶瓷等有腐蚀作用。与金属铝和锌、非金属硼和硅等反应放出氢;与氯、溴、碘等卤素发生歧化反应;与酸类起中和作用而生成盐和水。
氢氧化钠的电子式为Na+[:O:H]-。具体来说,Na+代表钠离子,而[:O:H]-则代表氢氧根离子。在这个电子式中,氧原子周围有8个电子,氢原子则有2个电子。氢氧原子间以共价键连接。这样的表示方式只适用于主族元素形成的物质,并不适用于过渡元素形成的物质。
氢氧化钠的电子式怎么写 naoh氢氧化钠的结构式的电子式是Na+[:O:H]-。
氢氧化钠的电子式为Na+[:OH]-,表示钠离子和氢氧根离子通过得失电子结合在一起,形成离子键。氢氧化钠,化学式为NaOH,俗称烧碱、火碱、苛性钠,是一种具有强腐蚀性的强碱,一般为片状和块状形态,易溶于水。
文章声明:以上内容(如有图片或视频亦包括在内)除非注明,否则均为网友提供,转载或复制请以超链接形式并注明出处。