初三上学期化学实验报告
- 实验:切下一小块蜡烛放入水中,发现蜡烛浮于水面,未溶解。- 结论:蜡烛密度小于水,不溶于水。 点燃时:- 观察:火焰分为三层,外层最亮,内层最暗。- 实验:火柴梗平放火焰中,外焰处变黑,焰心处无变化。- 实验:干燥玻璃杯和湿润内壁的玻璃杯分别罩在火焰上。
探究实验目的:对蜡烛在点燃前、点燃时和熄灭后的三个阶段进行细致的观察,学会完整地观察物质的变化过程及其现象。实验用品:一支新蜡烛、火柴、一支干净烧杯、水、水槽、澄清的石灰水、一把小刀。实验步骤与方法:1.观察蜡烛的颜色、形状、状态、硬度;嗅其气味。
通过这些实验现象,我们可以得出蜡烛燃烧的化学反应式为:石蜡+氧气→二氧化碳+水+碳。这表明蜡烛燃烧是一个复杂的化学反应过程,涉及到多种物质的生成和消耗。在实验过程中,我们还观察到了一些有趣的物理现象。例如,当火焰上方罩上烧杯时,可以看到烧杯内壁上的水滴,这说明蜡烛燃烧过程中产生了水蒸气。
实验报告:分为6个步骤:1):实验目的,具体写该次实验要达到的要求和实现的任务。(比如说,是要研究氢氧化钠溶液中加入硫酸铜溶液的反应状况)2):实验原理,是写你这次实验操作是依据什么来完成的,一般你的实验书上都有,你总结一下就行。
为了探究人体吸入的空气与呼出的气体的差异,我们进行了几个实验。首先,我们准备了两个空集气瓶,并用玻璃片盖好,以收集两瓶空气。接下来,将两个集气瓶装满水,用玻璃片盖住瓶口的一部分,然后慢慢往前推,直至完全覆盖瓶口,确保瓶内没有气泡残留。
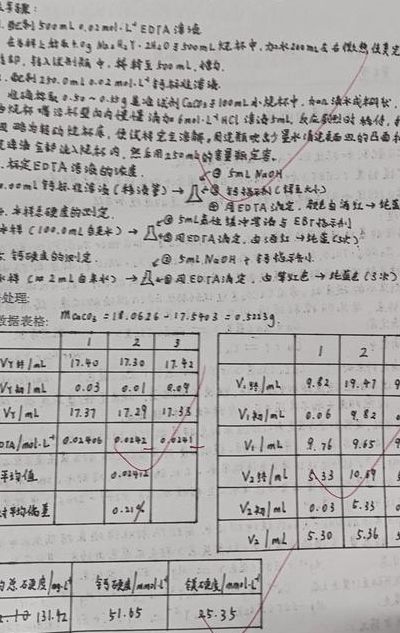
水中钙离子和镁离子含量及水硬的测定实验中产生误差的原因
1、分析方法和仪器的误差:分析方法和仪器的精度直接影响着实验结果的准确性。如果使用的分析方法不准确或者使用的仪器精度不高,就会对测定结果产生误差。水样取样和处理的误差:所测水样的取样和处理也造成误差。比如说,如果取样的时间不对,会导致水样中离子含量的变化。
2、如用基准氯化锌标定,则分析方法不一致,即分析的元素、缓冲溶液、PH值、指示剂、空白等等的不一致,导致较大的系统误差。镁离子与指示剂铬黑T的反应较钙离子灵敏,故常在滴定时加入少量的Mg2+-EDTA,使终点突跃。钙、镁是水中最常见离子,蒸馏水(去离子水)要严格处理。
3、测定水中钙镁含量时,控制溶液的pH值在10左右可以提高滴定的灵敏度。如果pH值过高,容易导致钙镁离子沉淀;而pH值过低时,镁离子与指示剂的络合较松散,可能导致滴定终点提前,从而引起较大偏差。因此,根据实际测定EDTA的酸效应,pH=10被认为是测定钙镁离子的最佳条件。
4、这样做对测定结果无影响,因为加少量Mg2+,在滴定过程中钙离子把镁离子从MgY中置换出来。其原理是:Mg2+与铬黑T形成酒红色配合物Mg-EBT,终点是颜色由酒红色变为纯蓝色,终点变色较为敏锐.。EDTA络合滴定法是一种测定水总硬度的化学分析方法。
水的硬度测定实验报告怎么写?
标定 标定的基准物有:金属Zn、ZnO、CaCO3等。Ca2++HIn2-=CaIn-+H+ Ca2++H2Y2-=CaY2-+2H+ CaIn-+H2Y2-=CaY2-+HIn2-+2H+ 红色 蓝色 测定 水的硬度是指水中除碱金属外的全部金属离子的浓度。
滴定前,溶液呈现红色,这是由于M-EBT的形成。当滴定至终点时,溶液颜色变为蓝色,表示MY和EBT的形成。在实验过程中,我们发现一些离子如Fe3+、Al3+等会干扰滴定结果,可通过三乙醇胺掩蔽;Cu2+、Pb2+、Zn2+等重金属离子则需使用KCN、Na2S或巯基乙酸进行掩蔽。
水的总硬度测定方法类似,需要移取一定量的水样至锥形瓶中,加入氨性缓冲溶液、三乙醇胺溶液和EBT指示剂,用EDTA标准溶液滴定至溶液由紫红色变为蓝色,记录滴定体积,重复三次。实验结果通过计算得出,Mg2+标准溶液和水的总硬度测定的浓度分别通过上述步骤得出,最终以三次测定的平均值表示。
用EDTA法怎么测定水的总硬度?用什么作指示剂?溶液的PH值应控制在什么...
1、水的总硬度=[Ca2+] + [Mg2+]. 可以用铬黑T作为指示剂,在pH=10的氨缓冲溶液中用EDTA直接滴定。另取一份样品。不用缓冲溶液,pH=13 时,Mg(OH)2沉淀,这时,EDTA只能滴定 Ca2+。
2、在使用EDTA滴定法测定水的总硬度时,控制溶液的酸度是至关重要的。通常,我们采用氨-氯化铵缓冲溶液或硼砂缓冲溶液来确保溶液的pH值维持在10±0.1的范围内,这对于滴定过程的准确性至关重要。
3、在采用EDTA进行水的硬度测定时,溶液的pH值需严格保持在12±0.1的范围内。EDTA络合滴定法是一种广泛应用的化学分析方法,用于测定水的总硬度。该方法基于在特定条件下,使用铬黑T作为指示剂和氨-氯化铵作为缓冲溶液,通过EDTA与水中的钙、镁离子反应形成稳定的络合物,以此确定水中钙镁离子的总量。
4、用EDTA测定水的总硬度时,以氨-氯化铵缓冲溶液,或硼砂缓冲溶液来控制溶液酸碱度(pH=10±0.1)。如果水样酸性或碱性太高时,可用氢氧化钠溶液或稀盐酸中和后,再用缓冲溶液来调整选择铬黑T或酸性铬蓝K作指示剂。
5、用edta法怎样测定水的总硬度如下:配制EDTA溶液:称取乙二胺四乙酸二钠盐,溶于水中,可适当加热溶解,冷却后转移至试剂瓶中,用水稀释至刻度,摇匀。绘制标准曲线:分别吸取一定浓度的钙离子和镁离子标准溶液,用EDTA溶液滴定,记录滴定量,绘制标准曲线。
6、用EDTA测定水的硬度时,溶液的pH值要控制在12±0.1的范围内。用EDTA测定水的硬度,即为EDTA络合滴定法,这是一种普遍使用的测定水的硬度的化学分析方法。它是在一定条件下,以铬黑T为指示剂,氨一氯化铵为缓冲溶液,EDTA与钙、镁离子形成稳定的配合物,从而测定水中钙、镁总量。
工业用水的总硬度测定的实验报告和演示
工业用水的总硬度测定实验中,我们主要学习了配位滴定法的原理和操作,深入理解了水硬度的概念及表示方法。通过实验,我们了解到硬水含有较高浓度的钙、镁离子,而测定这些离子的总量,就是测定水的总硬度。在实验中,我们使用了EDTA配位滴定法进行测定,该方法的核心在于溶液颜色的变化指示了滴定终点。
了解配位滴定法基本原理和方法。了解水的硬度的概念及其表示方法。实验原理 含有钙、镁离子的水叫硬水。
水的总硬度测定是化学分析中的一个重要实验,旨在了解水硬度的概念及其表示方法,同时掌握配位滴定的基本原理和方法。本实验通过测定水中钙、镁离子的总含量,来确定水的硬度。实验基于EDTA配位滴定法,该方法在滴定时,溶液颜色会从红色转变为蓝色,这标志着滴定终点的到达。
文章声明:以上内容(如有图片或视频亦包括在内)除非注明,否则均为网友提供,转载或复制请以超链接形式并注明出处。