氢氟酸能盛放在玻璃瓶中吗?原因是?:请用化学反应方程式和必要的文字...
根据4HF + SiO2 = SiF4↑ + 2H2O,所以氢氟酸不能保存在玻璃试剂瓶中.HF无色有刺激味的气体,在空气里易吸收水分呈现白雾。有剧毒。它的水溶液为氢氟酸。氢氟酸保存在塑料瓶中,不能保存在玻璃瓶中。
玻璃中含有大量的二氧化硅,氢氟酸在常温下能够与二氧化硅反应,所以不可以用玻璃瓶盛装氢氟酸,可以用塑料瓶盛装。
NaOH 与 SiO2 能反应:2 NaOH + SiO2 = Na2SiO3 + H2O 只是与 NaOH 反应的玻璃仅限于磨口玻璃。玻璃磨砂处 SiO2 暴露在外,能与NaOH 直接反应。
浓硝酸见光容易分解:4HNO3 = 4NO2↑ + O2↑ + 2H2O(条件为光照或加热),因此必须避光保存,不能装在无色玻璃瓶中。浓氨水挥发性很强,见光受热会大量挥发,使瓶内压强增大,有可能使瓶塞飞出或在打开瓶塞时有浓烈氨气喷出,也要避光保存。
因为氢原子和氟原子间结合的能力相对较强,使得氢氟酸在水中不能完全解离。
玻璃瓶能装氢氟酸吗
不可以。氢氯酸与玻璃会发生腐蚀反应。2NaOH + SiO2 = Na2SiO3 + H2O 。玻璃,以钠玻璃为例,可以写成Na2O.nSiO2,即主要成份是SiO2。
不能;因为玻璃的主要成分是硅酸钠,可以与氢氟酸发生化学反应;所以不能用玻璃瓶装氢氟酸。Na2SiO3+6HF=Na2SiF6+3H2O 氢氟酸需要密封在塑料瓶中,并保存于阴凉处。
氢氟酸(HF),会快速腐蚀玻璃,不能用玻璃瓶装。
不能放在玻璃瓶中,因为HF会腐蚀玻璃,正确的是用塑料瓶保存。
浓度很低的氢氟酸怎么保存,体积分数只有百分之一,可以保存在塑料瓶中,不能保存在玻璃瓶中,因为HF要与玻璃的主要成份SiO2反应。4HF + SiO2 = SiF4↑ + 2H2O,所以氢氟酸不能保存在玻璃试剂瓶中。
氢氟酸腐蚀玻璃的方程式
1、氢氟酸腐蚀玻璃的方程式为:SiO2 + 4HF = SiF4 + 2H2O。现在,让我们来详细解析这个反应。背景知识: 玻璃主要由硅酸盐矿物,如石英(SiO2)组成。因此,玻璃中的硅元素以二氧化硅(SiO2)的形式存在。
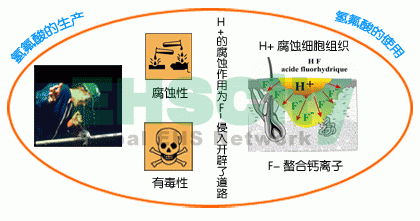
2、氢氟酸腐蚀玻璃的化学方程式为:4HF+SiO2==F2+Si+2H2O 拓展知识 氢氟酸(Hydrofluoric Acid)是氟化氢气体的水溶液,清澈,无色、发烟的腐蚀性液体,有剧烈刺激性气味。氢氟酸是一种弱酸,具有极强的腐蚀性,能强烈地腐蚀金属、玻璃和含硅的物体。如吸入蒸气或接触皮肤会造成难以治愈的灼伤。
3、氢氟酸腐蚀玻璃的化学方程式如下:SiO+4HF=SiF↑+2HO 该反应属于非氧化还原反应,因为反应前后各元素的化合价均未发生变化。
4、氢氟酸能够与玻璃中二氧化硅反应生成四氟化硅和水,方程式:SiO2(玻璃)+ H2 +热 SiH4(硅氢化物)+ H2O 补充:蚀刻玻璃是利用蚀刻剂(氢氟酸)来腐蚀刻制的玻璃,有文字或图案、花纹的蚀刻玻璃作为装饰品,美观大方,是建筑装饰常用的一种玻璃制品。
5、具体反应方程式为:4HF + SiO2 = SiF4 (气体)+ 2H2O如果HF酸比较多且浓,则生成的SiF4可以与HF进一步反应:2HF + SiF4 = H2[SiF6]生成氟硅酸(你将六个F看成四个O,则与硫酸相似了,也就是非金属原子形成的酸根)。
氢氟酸腐蚀玻璃的化学方程式
氢氟酸腐蚀玻璃的化学方程式如下:SiO+4HF=SiF↑+2HO 该反应属于非氧化还原反应,因为反应前后各元素的化合价均未发生变化。
氢氟酸腐蚀玻璃的方程式为:SiO2 + 4HF = SiF4 + 2H2O。现在,让我们来详细解析这个反应。背景知识: 玻璃主要由硅酸盐矿物,如石英(SiO2)组成。因此,玻璃中的硅元素以二氧化硅(SiO2)的形式存在。
氢氟酸腐蚀玻璃的化学方程式为:4HF+SiO2==F2+Si+2H2O 拓展知识 氢氟酸(Hydrofluoric Acid)是氟化氢气体的水溶液,清澈,无色、发烟的腐蚀性液体,有剧烈刺激性气味。氢氟酸是一种弱酸,具有极强的腐蚀性,能强烈地腐蚀金属、玻璃和含硅的物体。如吸入蒸气或接触皮肤会造成难以治愈的灼伤。
刻蚀玻璃的化学方程式如下:氢氟酸能够与玻璃中二氧化硅反应生成四氟化硅和水,方程式:SiO2(玻璃)+ H2 +热 SiH4(硅氢化物)+ H2O 补充:蚀刻玻璃是利用蚀刻剂(氢氟酸)来腐蚀刻制的玻璃,有文字或图案、花纹的蚀刻玻璃作为装饰品,美观大方,是建筑装饰常用的一种玻璃制品。
具体反应方程式为:4HF + SiO2 = SiF4 (气体)+ 2H2O如果HF酸比较多且浓,则生成的SiF4可以与HF进一步反应:2HF + SiF4 = H2[SiF6]生成氟硅酸(你将六个F看成四个O,则与硫酸相似了,也就是非金属原子形成的酸根)。
氢氟酸(HF)能否溶解钢化玻璃?
1、听起来可能很荒谬,尽管理论上氢氟酸是一种弱酸——这是因为氢原子和氟原子间结合的能力相对较强,使得氢氟酸在水中不能完全解离。但是氢氟酸却能够溶解很多其他酸都不能溶解的玻璃(二氧化硅),因此臭名昭著。
2、氢氟酸最好。因为生成气体四氟化硅,推动反应进行。能够提供氟离子的酸都能腐蚀玻璃。氢氟酸在工业上用来蚀刻玻璃。强碱如氢氧化钠,因为主要成分二氧化硅是酸性氧化物。因此氢氧化钠溶液不能用玻璃塞封存。
3、不管是钢化玻璃还是什么玻璃,凡是硅铝酸盐类的化合物,最怕的是氢氟酸。其中的二氧化硅,可以和氢氟酸生成六氟硅酸钠,三氧化二铝可以和氢氟酸生成四氟铝酸钠,全部给溶解掉。
4、当然是氢氟酸了,氢氟酸是氟化氢气体的水溶液,为无色透明至淡黄色冒烟液体,氢氟酸能够溶解很多其他酸都不能溶解的玻璃,所以也能融玻璃杯。
5、氢氟酸可以与玻璃中的二氧化硅(SiO2)反应,从而瓦解玻璃的结构,达到溶解目的。
为什么玻璃和氢氟酸酸反应发生
1、氢氟酸与玻璃反应生成SiF4,而氟化硅(SiF4)是无色、有毒、有刺激性臭味的气体。氢氟酸与玻璃反应生成SiF4挥发掉了,从而导致玻璃的腐蚀缺损,器到了雕刻玻璃的作用。
2、氢氟酸可以与玻璃中的二氧化硅(SiO2)反应,从而瓦解玻璃的结构,达到溶解目的。
3、玻璃,以钠玻璃为例,可以写成Na2O.nSiO2,即主要成份是SiO2。HF酸是唯一能与酸性氧化物起反应的酸,这是因为F的成键能力比O强,在这里Si-O键转化为Si-F键在能量上是有利的,再加上会生成SiF4气体,离开反应体系,因此会促进反应的进行。
4、氢氟酸与玻璃中的二氧化硅反应生成了水和氟化硅。氢氟酸是一种强腐蚀剂,能腐蚀玻璃、陶瓷、金属等物质。当氢氟酸与玻璃中的二氧化硅反应时,会生成四氟化硅和水,在玻璃表面形成一层霜状物。这种现象被称为“起霜”。
文章声明:以上内容(如有图片或视频亦包括在内)除非注明,否则均为网友提供,转载或复制请以超链接形式并注明出处。