v带和同步带改如何选择
平带传动:平带传动工作时,带套在平滑的轮面上,借带与轮面间的摩擦进行传动。v带传动:v带传动工作时,带放在带轮上相应的型槽内,靠带与型槽两壁面的摩擦实现传动。
v带选型图根据你得出的功率以及小带轮转速进行看图找点选择,若点在实线处则两种型号都可选择,点在虚线与虚线之间,可选离虚线较近的型号。虚线代表不同型号的V带。缺点:同步带的成本较高,且在使用过程中需要加强维护和更换,否则会影响传动精度。
V带和同步带各有千秋。V带像一个楔子嵌入在带轮中,可以提高驱动力并且不会像平带那样需要很大的张力。带轮的槽轮和V带接触面增大,也会使得跟随比平带好,而且带子一般不会偏离。但V带传动有打滑的风险,为了避免两个轴间输入和输出的打滑经常采用同步带。
V带:适用于中小功率传动和高速传动的场合。V带采用锥形设计,可使传动效率更高,同时在高速传动时噪音和振动较小。但是需要注意的是,V带的传动精度不如齿形同步带高。平面带:适用于低功率传动和低速传动的场合。平面带的传动效率较低,但其适用于传动功率较小的场合,且价格相对较低。
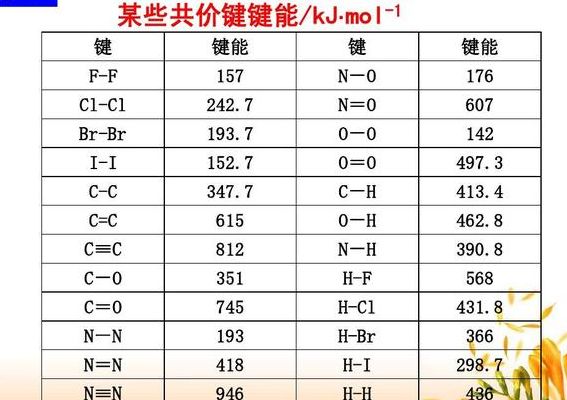
键能的定义
1、键能是指气态基态原子形成1mol化学键所释放的最低能量。01*10^5Pa和25摄氏度下(常温常压下),将1摩尔气态分子ab(g)离解成气态原子a(g)和b(g)所需的能量,用符号e表示,单位为kj.mol-1。键能越大,化学键越牢固,越难打断。
2、键能的定义:键能(Bond Energy)是从能量因素衡量化学键强弱的物理量。对双原子分子,键能为1mol气态分子离解成气态原子所吸收的能量。对多原子分子,键能为1mol气态分子完全离解成气态原子所吸收的能量分配给结构式中各个共价键的能量。
3、键能(Bond Energy)是从能量因素衡量化学键强弱的物理量。其定义为:在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ.mol-1。键能的数值通常用该温度下该反应的标准摩尔反应焓变表示,如不指明温度,应为2915K。
4、键能的概念是为对比键的强度提出来的。可以定义键能为在常温(298K)下基态化学键分解成气态基态原子所需要的能量。对于双原子分子,键能就是键离解能:对于多原子分子,所谓键能,就是一种统计平均值,或者说是近似值。键能的数据通常是通过热化学的方法得到的。键能的大小体现了键的强弱。
5、键能:定义:表征结合键牢固程度的物理量。对于双原子分子,在数值上等于把一个分子的结合键断开拆成单个原子所需要的能量。键能是断开或生成1mol化学键吸收或放出的能量 是化学键的基本性质 对反应的吸放热有影响 而活化能是发生化学反应分子必需达到的内能大小 控制反应速度自己在理解下。
6、①知识点定义来源&讲解:键能是指化学键成立所需要的能量,其大小取决于结合原子的电性和分子构型。 键能越高,表示结合越紧密,分子越稳定。该概念是从热力学角度来描述分子稳定性的。②知识点运用:键能可以用于预测分子的稳定性,即键能越大的化合物一般比键能小的化合物更加稳定。
什么是键能?
键能(Bond Energy)是从能量因素衡量化学键强弱的物理量。其定义为:在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ.mol-1。键能的数值通常用该温度下该反应的标准摩尔反应焓变表示,如不指明温度,应为2915K。
键能(bond energy)指的是在分子中形成或断裂一个键所需的能量。更高的键能通常意味着较强的化学键,因为其形成和断裂需要更多的能量。然而,并不是所有情况下都能简单地将键能与化合物的稳定性联系起来。稳定性是指分子或化合物在其环境中的相对不容易发生变化或分解的性质。
键能是化学键断裂或形成时释放或吸收的能量。键能指的是在化学反应中,当化学键断裂或形成时,会释放或吸收特定的能量。这是化学学科中的一个重要概念,对理解化学反应的过程和能量变化有着重要作用。在分子中,各个原子通过化学键连接在一起,这些化学键的强度和稳定性决定了键能的大小。
键能是什么?越大越稳定?
1、越小越稳定。它本身所具有的能量则与之不同,它本身所具有的能量越大,说明他和其他物质反应的能力越强,所以,它本身所具有的能量越大,它越不稳定。而键能是指破坏1mol化学键所需要的能量,因此,键能越大,说明破坏之所需要的能量越大,他就越不容易被破坏。
2、键能就是化学键的 能量,能量越大就越稳定,不容易分开,单质之间也要看是什么键才能说什么键能,如果是双原子就是原子之见距离越小键能越大,原子大小越小 见能就大。
3、物质是由原子或分子相互结合而组成的,在原子和分子相互结合的过程中,原子,分子之间就会有力的作用而使得原子分子之间的相互稳定构成宏观物质。这个力的作用用能量的方式来衡量就是键能。键能越大说明原子分子之间的作用力也越大,要破坏这个化学键所需要的能量输入也就越大。
4、①知识点定义来源&讲解:键能是指化学键成立所需要的能量,其大小取决于结合原子的电性和分子构型。 键能越高,表示结合越紧密,分子越稳定。该概念是从热力学角度来描述分子稳定性的。②知识点运用:键能可以用于预测分子的稳定性,即键能越大的化合物一般比键能小的化合物更加稳定。
5、物质的化学性质就越稳定。键能(Bond Energy)是从能量因素衡量化学键强弱的物理量。其定义为:在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g),B(g)所需的能量,用符号E表示,单位为kJ.mol-1。键能的数值通常用该温度下该反应的标准摩尔反应焓变表示,如不指明温度,应为2915K。
文章声明:以上内容(如有图片或视频亦包括在内)除非注明,否则均为网友提供,转载或复制请以超链接形式并注明出处。